[정정청구항]
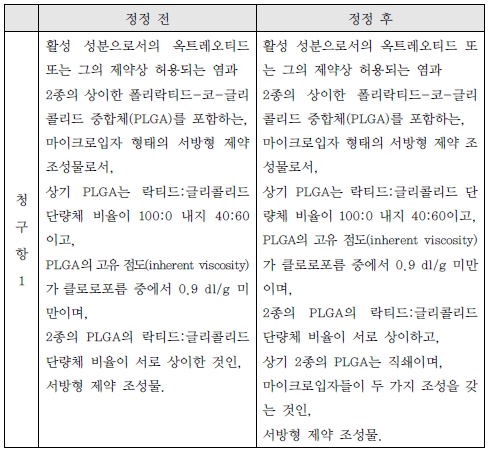
[기재표]

[표 4]

| 사건번호 | 2014허3590 등록무효(특) |
|---|---|
| 판례제목 | 2014허3590 등록무효(특) |
| 출원번호 | 제1245919호 |
| 분야 | 특허/실용신안 |
| 판결일 | 2016-02-04 |
| 법원명 | 특허법원 |
| 원고 | 동국제약 주식회사 |
| 피고 | 노파르티스 아게 |
| 판사 | 한규현, 손천우, 윤주탁 |
| 판결결과 | 등록무효 |
| 주문 | 1. 특허심판원이 2014. 4. 30. 2013당1870호 사건에 관하여 한 심결 중 특허 등록번호 제1245919호 발명의 청구항 1, 3 내지 5, 7 내지 13 부분을 취소한다. 2. 소송비용은 피고가 부담한다. |
| 청구취지 | 주문과 같다. |
| 기초사실 | 가. 이 사건 정정발명 1) 발명의 명칭 : 옥트레오티드 및 2종 이상의 폴리락티드-코-글리콜리드 중합체를 포함하는 서방형 제제 2) 국제출원일/ 우선권주장일/ 특허법 제203조의 서면 제출일/ 등록일/ 특허등록번호 : 2006. 12. 20./ 2005. 12. 22./ 2008. 6. 20./ 2013. 3. 14./ 제1245919호 3) 특허권자 : 피고 4) 특허청구범위(2015. 7. 8.자 정정심결로 확정된 것. 이하에서는 정정된 청구항들을 ‘정정청구항 1’과 같은 방법으로 칭한다) 【청구항 1】활성 성분으로서의 옥트레오티드 또는 그의 제약상 허용되는 염과 2종의 상이한 폴리락티드-코-글리콜리드 중합체(PLGA)를 포함하는, 마이크로입자 형태의 서방형 제약 조성물로서, 상기 2종의 PLGA 중 1종은 락티드:글리콜리드 단량체 비율이 75:25이며 다른 1종은 락티드:글리콜리드 단량체 비율이 100:0 내지 40:60이고, PLGA의 고유 점도(inherent viscosity)가 클로로포름 중에서 0.9 dl/g 미만이며, 2종의 PLGA의 락티드:글리콜리드 단량체 비율이 서로 상이하고, 상기 2종의 PLGA는 직쇄이며, 상기 2종의 PLGA 각각의 중량이 2종의 PLGA 전체 중량의 적어도 30%이고, 각 마이크로입자는 상기 2종의 PLGA 중 1종만을 포함하고 있어 마이크로입자들이 두 가지 조성을 갖는 것인, 서방형 제약 조성물. 【청구항 2】(판단 대상이 아니므로 기재를 생략한다) 【청구항 3】제1항 또는 제2항에 있어서, 상기 다른 1종의 PLGA의 락티드:글리콜리드 단량체 비율이 90:10 내지 40:60인 제약 조성물. 【청구항 4】제1항 또는 제2항에 있어서, 상기 다른 1종의 PLGA의 락티드:글리콜리드 단량체 비율이 65:35인 제약 조성물. 【청구항 5】제1항 또는 제2항에 있어서, PLGA의 고유 점도(inherent viscosity)가 클로로포름 중에서 0.8dl/g 미만인 제약 조성물. 【청구항 6】(정정심판에 의해 삭제) 【청구항 7】제1항 또는 제2항에 있어서, 활성성분이 옥트레오티드의 파모에이트 염인 제약 조성물. 【청구항 8】제1항 또는 제2항에 있어서, 마이크로입자의 직경이 10㎛ 내지 90㎛인 제약 조성물. 【청구항 9】제1항 또는 제2항에 있어서, 마이크로입자가 추가로 항-응집제(anti-agglomerating agent)와 혼합되거나, 항-응집제로 덮히거나, 항-응집제로 코팅되는 것인 제약 조성물. 【청구항 10】제9항에 있어서, 항-응집제가 만니톨인 제약 조성물. 【청구항 11】제1항 또는 제2항에 있어서, 감마선 조사에 의해 멸균된 제약 조성물. 【청구항 12】제1항 또는 제2항에 있어서, 말단비대증 환자의 장기간 유지요법, 및 악성 카르시노이드 종양 및 혈관작용성 장 펩티드(vasoactive intestinal peptide) 종양[VIP종(vipoma) 종양]과 관련된 심한 설사와 홍조의 치료를 위해 사용되는 제약 조성물. 【청구항 13】바이알 중의 제1항 또는 제2항에 따른 제약 조성물을, 앰플, 바이알 또는 프리필드(prefilled) 주사기 중의 수성 비히클과 함께 포함하거나, 또는 마이크로입자로서의 상기 제약 조성물과 비히클을 이중 챔버 주사기에 분리시켜 포함하는 투여 키트. 5) 발명의 개요 본 발명은 활성 성분으로서의 옥트레오티드 또는 그의 제약상 허용되는 염과 2종 이상의 상이한 폴리락티드-코-글리콜리드 중합체(PLGA)를 포함하는 서방형 제제에 관한 것이다. 본 발명의 제약 조성물은 말단비대증 환자의 장기간 유지 요법이나, 악성 카르시노이드 종양, 혈관작용성 장 펩티드(vasoactive intestinal peptide) 종양[VIP종(vipoma) 종양]과 관련된 심한 설사와 홍조의 치료를 위해 처방되는 펩티드 약물이다. 펩티드 약물은 통상 전신적으로, 예를 들어 비경구로 투여된다. 그러나, 비경구 투여는 통증이 있고, 특히 매일 반복 투여해야 하기 때문에 불쾌감을 일으킬 수 있다. 환자에게 주사하는 횟수를 최소화하기 위해 약물물질은 데포(depot) 제제로 투여되어야 한다. 주사 가능한 데포 제제가 갖는 통상적인 결점은 전체 방출 기간 동안 0에 가까운 혈장 수준, 높은 피크 수준과 같은 혈장 수준의 변동이다. 혈장 수준의 변동은 본 발명에 따른 제약 조성물에서 2종 이상의 상이한 PLGA의 적합한 조합물을 사용함으로써 유의하게 감소될 수 있으며, PLGA의 락티드:글리콜리드 단량체 비율은 100:0 내지 40:60, 바람직하게는 90:10 내지 40:60, 보다 바람직하게는 85:15 내지 65:35이다. 본 발명에 따른 제약 조성물은 데포 혼합물이거나, 조성, 분자량 및/또는 중합체 구조의 관점에서 상이한 중합체의 중합체 블렌드일 수 있다. 본 발명에서, 중합체 블렌드는 하나의 임플란트 또는 마이크로입자 중 2종 이상의 상이한 중합체의 고용체 또는 현탁액으로 정의된다. 대조적으로, 데포의 혼합물은 본원에서 각 데포에 1종이상의 PLGA를 갖는 상이한 조성의 임플란트, 마이크로입자 또는 반고체 제제와 같은 2종 이상의 데포의 혼합물로 정의된다. PLGA가 중합체 블렌드로 존재하는 제약 조성물이 바람직하다. 한편, 이 사건 정정발명의 설명에는 정정청구항 1에 해당하는 실시례로 마이크로입자들이 두 가지 조성을 갖는 ‘실시예 1-10’이 기재되어 있는데, 위 실시례에서는 2종의 마이크로입자들이 서로 상이한 PLGA를 갖고, PLGA는락티드:글리콜리드 단량체 비율이 65:35 이거나 75:25로 서로 상이하며, 위 2종의 PLGA는 30:70의 중량비를 갖고 있다. 또한, 위 ‘실시예 1-10’의 마이크로입자 조성물을 토끼에게 근육 주사하여 투여 후 96일까지 혈장수준을 측정한 결과가 기재되어 있다. 나. 선행발명들 1) 선행발명 1 (갑 제5호증) 2005. 1. 13. 공고된 등록특허공보 제10-0466637호에 게재된 ‘서방성 미립구의 혼합 제형을 연속한 단일 공정으로 제조하는 방법’에 관한 발명이다. 2) 선행발명 2 (갑 제6호증) 1990. 1. 30. 공고된 미국 특허공보 제4,897,268호에 게재된 ‘약물 전달 시스템 및 그 제조 방법(Drug delivery system and method of making the same)’에 관한 발명이다. 3) 선행발명 3 (갑 제7호증) 2013. 2. 18. 공고된 등록특허공보 제1233892호에 게재된 ‘소마토스타틴 유사체를 포함하는 미소입자’에 관한 발명이다. 4) 선행발명 6 (갑 제8호증) 2003. 7. 22. 공고된 등록특허공보 제392501호에 게재된 ‘다중 에멀젼법에 의한 서방출성 미립구의 제조방법’에 관한 발명이다. 5) 선행발명 7 (갑 제41호증) 2005. 8. 30. 공개된 공개특허공보 제10-2005-0086708호에 게재된‘옥트레오티드 마이크로입자를 포함하는 약제학적 조성물’에 관한 발명이다. 다. 심결의 경위 1) 원고는 특허심판원에 2013당1870호로 피고를 상대로 “이 사건 특허발명의 청구항 1, 3 내지 6, 8 내지 10, 12는 선행발명 1에 의해 신규성이 부정되거나, 이 사건 특허발명의 청구항 1, 3 내지 13은 그 발명이 속하는 기술분야에서 통상의 지식을 가진 사람(이하 ‘통상의 기술자’라 한다)이 선행발명 1, 2 등으로부터 용이하게 발명할 수 있으므로, 그 등록이 무효로 되어야 한다.”는 등의 이유를 들어 이 사건 특허발명에 대한 무효심판을 청구하였다. 2) 피고는 2014. 2. 10. 위 무효심판절차에서 이 사건 특허발명의 청구항 1을 아래 표 기재와 같이 정정을 구하는 것을 포함하여 이 사건 특허발명의 청구범위를 정정하는 내용의 정정청구를 하였다(정정 후의 특허발명의 각 청구항을 ‘2014. 2. 10.자 정정청구항 1’과 같은 방법으로 표시한다). 3) 특허심판원은 2014. 4. 30. “피고의 2014. 2. 10.자 정정청구는 적법하다. ‘2014. 2. 10.자 정정청구항 1’은 선행발명 1, 2에 의해 신규성과 진보성이 부정되지 않는다. 또한 ‘2014. 2. 10.자 정정청구항 3 내지 5, 7 내지 13’은 ‘2014. 2. 10.자 정정청구항 1’의 종속항으로서 위 청구항의 구성을 모두 포함하고 있으므로, ‘2014. 2. 10.자 정정청구항 1’의 신규성과 진보성이 부정되지 않는 이상, 신규성과 진보성이 부정되지 않는다.”는 등의 이유로 원고의 심판청구를 기각하는 이 사건 심결을 하였다. 4) 피고는 2014. 5. 29. 이 사건 특허발명의 청구범위를 위 2)항의 정정청구항과 같이 정정하는 내용의 정정심판을 청구하였다. 특허심판원은 위 정정심판청구사건을 2014정51호로 심리한 후 2014. 6. 20. 위 정정심판청구를 인용하는 심결을 하였으며, 위 정정심결은 그 무렵 확정되어 정정공고가 이루어졌다. 5) 2014. 12. 2. 위 4)항에 따라 정정된 정정발명의 청구범위를 위 ‘1의 가. 4)항’과 같이 정정하는 내용의 정정심판을 청구하였다. 특허심판원은 위 정정심판청구사건을 2014정132호로 심리한 후 2015. 7. 8. 위 정정심판청구를 인용하는 심결을 하였으며, 위 정정심결은 그 무렵 확정되어 정정공고가 이루어졌다(이하 ‘이 사건 정정발명’이라 한다). 【인정근거】다툼 없는 사실, 갑 제1 내지 8, 41호증, 을 제1, 29, 30호증, 변론 전체의 취지 |
| 원고의 주장요지 | 가. 신규성 정정청구항 1, 3 내지 5, 9, 10, 12는 선행발명 1 또는 6에 의하여 신규성이 부정된다. 나. 진보성 1) 정정청구항 1, 3 내지 5, 9, 10, 12는 선행발명 1에 의하여 또는 선행발명 6에 의하여 또는 선행발명 1, 2, 6에 의하여 또는 선행발명 1, 2, 7에 의하여 각 진보성이 부정된다. 2) 정정청구항 7, 8, 11, 13은 선행발명 1, 3에 의하여 또는 선행발명 6, 3에 의하여 각 진보성이 부정된다. 다. 발명의 설명 기재 요건 등 1) 구 특허법(2007. 1. 3. 법률 제8171호로 개정되기 전의 것. 이하 ‘구 특허법’이라 한다) 제42조 제3항 위배 가) 정정청구항 1, 3 내지 5, 7 내지 13(이하 ‘이 사건 각 정정청구항’이라 한다)이 인간이나 토끼에 대하여 치료적 범위 내의 혈중농도31)가 3개월 이상 지속되는 효과가 있다고 하려면, 인간이나 토끼에 대한 치료적 범위 내의 혈중농도가 어느 정도인지 확인되어야 하고, 이 사건 각 정정청구항의 조성물을 투여하였을 때 그와 같은 치료적 범위 내의 혈중농도가 3개월 이상 지속되는 것이 시험례로 기재되어 있거나 또는 이에 대신할 수 있을 정도로 구체적으로 기재되어야 있어야 할 것인데, 이 사건 정정발명의 명세서에는 그와 같은 기재를 발견할 수 없다. 따라서, 이 사건 각 정정청구항은 약리효과의 기재에 관한 명세서 기재요건을 충족하지 못하였으므로, 구 특허법 제42조 제3항에 위배된다. 나) 이 사건 정정발명의 명세서에는 약물의 방출 지속 기간에 매우 중요한 영향을 미치는 약물의 부하율 등에 대한 한정이 되어 있지 않아, 이 사건 각 정정청구항은 발명의 설명이 통상의 기술자가 쉽게 실시할 수 있도록 명확하고 상세하게 기재되어 있지 않으므로 구 특허법 제42조 제3항에 위배된다. 다) 설령, ‘실시예 1-10’에서의 혈중농도 변화가 3개월 이상의 치료적 범위를 보여주고 있다고 하더라도, 이 사건 각 정정청구항은 발명의 설명에서 단량체 비율을 65:35, 75:25로, 고유 점도를 0.6dl/g, 0.4dl/g로 한정하고 있는 하나의 실시례(‘실시예 1-10’)만을 보여주고 있을 뿐, 발명의 설명에서 청구범위에서 한정하고 있는 수치범위 전체에 걸쳐 위와 같은 효과를 갖고 있는지를 보여주지 못하고 있다. 따라서, 이 사건 각 정정청구항은 구 특허법 제42조 제3항에 위배된다. 2) 구 특허법 제42조 제4항 제1호 위배 단량체 비율을 65:35, 75:25로, 고유 점도를 0.6dl/g, 0.4dl/g로 한정하고 있는 하나의 실시례(‘실시예 1-10’)만으로는 단량체 비율과 고유 점도가 다른 이 사건 각 정정청구항의 모든 조성물들에 대하여 권리범위를 확장할 수 없어, 이 사건 각 정정청구항은 청구범위가 발명의 설명에 의해 뒷받침되지 않으므로 구 특허법 제42조 제2항 제1호에 위배된다. 라. 심결의 위법 따라서, 이 사건 심결은 이와 결론을 달리하여 위법하므로 취소되어야 한다. |
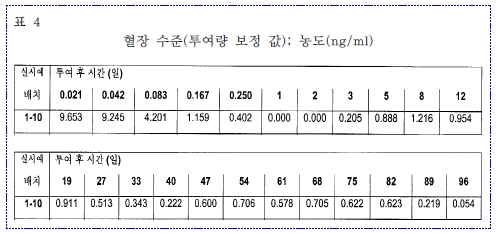
| 이 사건 심결의 당부에 대한 판단 | <구 특허법 제42조 제3항 위배 여부> 가. 판단의 대상 먼저, 통상의 기술자가 이 사건 각 정정청구항(정정청구항 3 내지 5, 7 내지 13은 정정청구항 1을 직․간접적으로 인용하고 있는 종속항이다)을 용이하게 실시할 수 있을 정도로 이 사건 각 정정청구항의 효과가 이 사건 정정발명의 설명에 기재되어 있지 않아 구 특허법 제42조 제3항에 위배되는지를 보기로 한다. 나. 이 사건 각 정정청구항의 효과 이 사건 정정발명의 아래와 같은 명세서 기재를 종합하면, 이 사건 각 정정청구항의 효과는 ‘3개월 초과 기간 동안 말단비대증, 악성 카르시노이드 종양, 혈관작용성 장 펩티드 종양(이하 ‘이 사건 각 질병’이라 한다) 치료용의약물질(활성성분)인 옥토레오티드를 혈중농도의 변동이 작고 혈중농도가 치료적 범위 내에 있을 정도로 지속적으로 방출하는 서방형 제제로서의 의약조성물을 제공하는 것’이라고 할 것이다(피고도 위와 같은 취지로 이 사건 각 정정청구항의 효과를 주장하고 있는 것으로 보인다). 다. 용이하게 실시할 수 있을 정도로 효과가 기재되어 있는지 여부 1) 판단에 필요한 법리 구 특허법 제42조 제3항은 “발명의 상세한 설명에는 통상의 기술자가 용이하게 실시할 수 있을 정도로 그 발명의 목적․구성 및 효과를 기재하여야 한다”고 규정하고 있는바, 그 뜻은 특허출원된 발명의 내용을 제3자가 명세서만으로 쉽게 알 수 있도록 공개하여 특허권으로 보호받고자 하는 기술적 내용과 범위를 명확하게 하기 위한 것이므로 통상의 기술자가 당해 발명을 명세서 기재에 의하여 출원시의 기술수준으로 보아 과도한 실험이나 특수한 지식을 부가하지 않고서도 정확하게 이해할 수 있고 동시에 재현할 수 있는 정도를 말하는 것이다(대법원 2005. 11. 25. 선고 2004후3362 판결, 대법원 2011. 10. 13. 선고 2010후2582 판결 등 참조). 한편, 일반적으로 기계장치 등에 관한 발명에 있어서는 특허출원의 명세서에 실시예가 기재되지 않더라도 통상의 기술자가 발명의 구성으로부터 그 작용과 효과를 명확하게 이해하고 용이하게 재현할 수 있는 경우가 많으나, 이와는 달리 이른바 실험의 과학이라고 하는 화학발명의 경우에는 당해 발명의 내용과 기술수준에 따라 차이가 있을 수는 있지만 예측가능성 내지 실현가능성이 현저히 부족하여 실험데이터가 제시된 실험예가 기재되지 않으면 통상의 기술자가 그 발명의 효과를 명확하게 이해하고 용이하게 재현할 수 있다고 보기 어려운 경우가 많다(대법원 2001. 11. 30. 선고 2001후65 판결 등 참조). 2) 구체적 판단 가) 이 사건 각 정정청구항 발명의 본질과 명세서 기재 정도 이 사건 각 정정청구항 발명의 본질은, 단순히 의약물질(활성성분)인 옥토레오티드와 2종의 상이한 폴리락티드-코-글리콜리드 중합체(PLGA) 등을 포함하면서 이 사건 각 정정청구항에서 한정하고 있는 것과 같은 단량체 비율과 고유 점도 등을 가진 새로운 조성물을 발명하였다는 점에만 있는 것이 아니라, 위 나.항에서 본 바와 같이 위와 같은 새로운 조성물이 3개월 초과의 방출기간 동안 이 사건 각 질병을 치료하는 의약물질(활성성분)인 옥토레오티드를 혈중농도 변동이 작고 혈중농도가 치료적 범위 내에 있을 정도로 지속적으로 방출함으로써 이 사건 각 질병에 대한 장기간의 치료 효과를 갖는 조성물을 발명하였다는 점에 있다고 할 것이다. 결국 이와 같은 발명에 장기간의 독점권을 부여하는 것이 정당화 되려면, 위 발명이 기존의 기술수준을 의미 있는 정도로 향상시켰을 것이 필요하고(이는 진보성의 판단에서 다루어져야 할 것이다), 위 발명의 고유한 기술적 의미를 인식할 수 있도록 공중에게 발명을 충분히 공개하여야 한다. 따라서, 통상의 기술자가 이 사건 각 정정청구항의 고유한 기술적 의미를 인식할 수 있도록 하기 위해서는, 명세서 기재에 의하여 출원 당시의 기술수준으로 보아 과도한 실험이나 특수한 지식을 부가하지 않고서도 이 사건 각 정정청구항의 조성물이 이 사건 각 질병에 대하여 장기간의 치료 효과를 갖는다는 것을 정확하게 이해할 수 있도록 발명을 공개하여야 할 것이다. 나) 옥토레오티드 약리효과로부터의 예측 가능성 흡수율, 용출률 등을 개선하기 위하여 약리기전 등 약리효과가 밝혀져 있는 공지된 의약물질(활성성분)에 코팅 등 제제의 물리적 형태에 기술적 특징이 있는 구성을 추가하는 정도의 제형발명에 있어서는 흡수율, 용출률 등이 개선되었는지를 보여주는 시험례가 기재되어 있으면, 통상의 경우 통상의 기술자가 과도한 실험이나 특수한 지식을 부가하지 않고서도 위 제형발명으로서의 효과를 이해할 수 있을 것으로 보인다. 이에 비하여, 이 사건 각 정정청구항의 서방형 제제와 같이 장기간 지속적으로 효과가 나타나도록 하기 위하여 방출 특성을 조절할 목적으로 의약물질(활성성분)인 옥토레오티드가 2종의 상이한 폴리락티드-코-글리콜리드 중합체(PLGA) 등과 함께 새로운 조성물을 형성한 경우, 의약물질(활성성분)인 옥토레오티드에 대하여 약물의 방출 특성이 조절되지 않았을 때의 약리기전 등 약리효과가 밝혀져 있다고 하더라도, 3개월 초과의 방출기간 동안 이미 밝혀진 옥토레오티드의 약리효과가 지속적으로 나타날지를 예측하기는 상당히 어려울 것으로 보인다(다만, 혈중농도가 치료영역33) 범위 내에서 일정하게 유지되는 등의 특별한 경우에는 예측가능성이 높아질 수 있을 것이다). 다) 이 사건 정정발명의 명세서 기재에 기초한 효과의 인식 가능성 (1) 이 사건 정정발명의 명세서 기재 이 사건 정정발명의 명세서의 표 4에는 이 사건 각 정정청구항의 보호범위에 포함되는 ‘실시예 1-10’의 조성물을 토끼에게 주사하고 96일간 토끼 혈장에서의 옥토레오티드 농도를 측정한 아래 표와 같은 데이터가 포함되어 있다(이하 ‘이 사건 시간․농도데이터’라 한다). 위 표에는 대부분의 일자에서의 혈중농도가 0.2ng/ml 이상으로 기재되어 있으나, 제1, 2일의 혈중농도는 0으로 기재되어 있다. (2) 피고의 주장 이와 관련하여, 피고는 “인간에 대한 시간․농도데이터와 토끼에 대한 시간․농도데이터를 비교해 보면, 인간에 대한 혈중농도 곡선은 토끼에 대한 혈중농도 곡선과 대비하여 형상은 유사하면서도, 약물 방출이 더 오래 지속되고 지체기의 혈장 농도가 증가하는 등 전체적으로 더 길게 늘어지면서 평평한 형태를 보이므로, 어떤 제형이 약 3개월의 기간 동안 토끼에 대하여 지속적으로 적절한 수준의 약물 방출을 나타내는 것으로 확인되면, 인간에 대해서도 3개월 제형으로 사용되기에 좋은 가능성이 있는 것으로 판단할 수 있다. ‘이 사건 시간․농도데이터’를 살펴보면, ㉠ 약물이 3개월 이상인 96일에 이르기까지 지속적으로 방출되고, 특히 89일에도 혈중농도가 0.219ng/ml에 이르는 등 뚜렷한 수준의 약물 방출이 이어지고 있으며[경험적으로 옥트레오티드에 대한 토끼 실험에 있어서의 0.2ng/ml 정도의 혈중농도는 인간에 대한 최소 치료 농도에 상응하고, Cmin값이 0.2 ng/ml에 비하여 너무 낮지 않고 너무 오래 지속되지 않으면 그러한 골짜기(valley) 구간은 약물농도가 정상 상태(steady state)에 도달하였을 때(통상 3 내지 7회 주사 후에 도달) 보상될 것으로 합리적으로 예상할 수 있다], ㉡ 제1 지체기가 단 이틀에 불과할 뿐만 아니라(제1일과 제2일), 제3일째부터는 혈중농도가 다시 상당한 수준(0.2ng/ml)으로 회복되었으며, ㉢ ‘확산 방출’과 ‘침식 방출’ 시기의 최고혈중농도(Cmax)와 최저혈중농도(Cmin)(제2 지체기)의 비율이 서방형 제제의 생체 내 데이터로서 좋은 결과인 10배 이내에 불과하다(1.216/0.222).”는 이유를 들어 ‘이 사건 시간․농도 데이터’가 3개월 서방형 제제로서 좋은 후보가 될 수 있다고 주장하고 있다. (3) 효과의 인식 가능성(피고 주장에 대한 판단) (가) ‘이 사건 시간․농도데이터’는 비록 토끼에 대한 시험 결과이기는 하나, 시간에 따른 약물의 혈중농도만을 보여주고 있을 뿐 이 사건 각 정정청구항의 조성물이 토끼에 대하여 장기간에 걸쳐 이 사건 각 질병 치료의 효과가 있는지 여부를 직접 보여주지는 못하고 있다. (나) 한편, 피고가 주장하고 있는 위 ㉠ 내지 ㉢항과 같은 사정들을 근거로, 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도, ‘이 사건 시간․농도데이터’를 기초로 이 사건 각 정정청구항의 조성물이 장기간에 걸쳐 이 사건 각 질병에 대하여 치료 효과가 있음을 인식할 수 있었다고 보려면, 적어도 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도, ⓐ 토끼에 대한 시간․농도데이터를 기초로 인간에 대한 장기간의 치료효과를 직접 판단할 수 있었거나, ⓑ 토끼에 대한 시간․농도데이터를 기초로 인간에 대한 혈중농도 양상을 추정할 수 있었고 동시에 위와 같은 추정을 기초로 인간에 대한 장기간의 치료 효과를 판단할 수 있었음이 전제되어야 할 것이다. (다) 갑 제50호증, 을 제11, 31호증의 각 기재와 증인 마이크 커 후의 증언 및 변론 전체의 취지를 종합하면, 통상의 기술자가 이 사건 정정발명의 우선일 당시 말단비대증을 치료하기 위한 옥토레오티드 서방형 제제에 있어 최소유효농도가 1ng/ml임을 인식할 가능성이 높았던 것으로 보인다(다만 최소독성농도에 대하여는 특별한 기준을 인식하기 어려웠던 것으로 보인다). (라) 그러나, 기록상 제출된 증거만으로는 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도 토끼에 있어서의 혈중농도 0.2ng/ml가 인간에 있어서의 최소유효농도에 상응하는 것으로 인식할 수 있었다고 보기 어렵다(특히 피고 주장 ㉠, ㉡항과 관련하여. 이에 대하여 증인 마이크 커 후는 0.2ng/ml가 피고 회사 내부의 잠재적인 기준이라는 취지로 증언하였는바, 피고 회사 내부의 잠재적인 기준은 통상의 기술자가 과도한 실험이나 특수한 지식을 부가하지 않고서도 인식할 수 있었던 사항이라고 보기 어렵다. 한편, 을 제34호증의 명세서에는 “래비트에게 체중 kg당 5mg의 투여량으로 옥트레오티드 서방형 제제를 근육내로 투여하였을 때 0.3ng/ml 이상 20ng/ml 이하의 옥트레오티드 농도를 나타낸다.”고 기재되어 있기는 하나, 이러한 기재만으로 통상의 기술자가 토끼에 있어서의 혈중농도 0.2ng/ml가 인간에 있어서의 최소유효농도에 상응한다고 인식할 수 있었다고 보기 어렵다). 따라서, 통상의 기술자가 ‘이 사건 시간․농도데이터’를 기초로 ‘실시예 1-10’의 조성물이 인간에게 투여되었을 경우 적어도 제1, 2일을 제외한 나머지 일자에 있어 최소혈중농도인 1ng/ml이상의 혈중농도[위 (다)항 참조]를 가질 것으로 인식할 수 있었다고 보기 어렵다. (마) 또한, 기록상 제출된 증거만으로는 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도 토끼에 대한 시간․농도데이터로부터 인간에 대한 장기간의 치료 효과를 직접 판단할 수 있었다고 보기 어렵다[위 (나)의 ⓐ항 참조]. (바) 더불어 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도, ‘이 사건 시간․농도데이터’와 같은 토끼에 대한 시간․농도데이터를 기초로 인간에 대한 혈중농도 양상을 추정할 수 있었다고 보기 어렵다(증인 마이크 커 후는 “결과적으로 얼마만큼의 투여 용량 수준과 농도 수준이 인간의 경우 나올지는 직접 임상시험을 해봐야 알 수 있다.”는 취지로 증언하였고, 갑 제25호증에도 “토끼 체내에 대한 PK 데이터는 인간에 대한 임상 PK 연구를 항상 정확히 반영하지 않고 인간에 대한 임상 PK 연구를 대체할 수도 없다.”고 기재되어 있다. 위 (나)의 ⓑ항 참조]. 더욱이 설령 통상의 기술자가 토끼에 대한 시간․농도데이터를 기초로 인간에 대한 혈중농도 양상을 추정할 수 있었다고 하더라도, 혈중농도가 치료영역 범위 내에서 일정하게 유지되는 등의 특별한 경우를 제외하고는 통상의 기술자가 인간에 대한 혈중농도 양상을 기초로 인간에 대한 장기간의 치료효과를 판단하는 것이 용이하였다고 보기 어렵다[증인 마이크 커 후는 “서방형 제제에 대하여 보건 당국이 신약 승인과 관련하여 사용하는 공통된 기준이 없는 것으로 알고 있다. 각 승인되는 대상인 약물마다 특이하게 결정을 하는 것으로 알고 있다. 그렇지만 어떤 신약 승인이라 할지라도 두 가지 중요한 고려사항이 있는데, 첫 번째가 약물의 효능이고, 두 번째가 약물의 안전성이다. 서방형의 경우에도 예외가 아니어서 환자에게서 임상학적으로 효능이 있고, 안전하다는 것을 증명할 수 있다면 보건당국으로부터 승인을 받을 수 있다.”는 취지로 증언하였다. 위 (나)의 ⓑ항 참조]. 따라서, 통상의 기술자가 이 사건 정정발명의 우선일 당시 과도한 실험이나 특수한 지식을 부가하지 않고서도 ‘이 사건 시간․농도데이터’를 기초로 인간에 혈중농도 양상을 추정하고 나아가 인간에 대한 장기간의 치료 효과를 용이하게 판단할 수 있었다고 보기 어렵다. (사) 그렇다면, 방출기간 중 일부 구간에 있어 최소혈중농도에 미치지 못하는 일자가 있는 경우(특히 ‘이 사건 시간․농도데이터’의 경우 제1, 2일에 혈중농도가 0이다) “싱글 도스[single dose, 단회(單回) 투여]에 있어 비록 단기간에 목표하는 수준 이하로 혈중농도가 나오는 경우가 있다고 하더라도, 멀티플 도스[multiple dose, 다회(多回) 투여]를 통하여 스테디 스테이트(steady state, 정상 상태)에 이르게 되면, 위와 같은 수준 이하의 부족한 혈중농도를 보상해 줄 수 있어 크게 우려할 사항이 아니다.”는 취지의 증인 마이크 커 후의 증언이 통상의 기술자가 용이하게 인식할 수 있었던 사항에 해당한다고 보더라도, 위 (가) 내지 (바)항과 같은 사정들에 비추어 보면, 이 사건 정정발명의 우선일 당시 통상의 기술자가 과도한 실험이나 특수한 지식을 부가하지 않고서도 ‘이 사건 시간․농도데이터’를 기초로 ‘실시예 1-10’을 포함한 이 사건 각 정정청구항이 이 사건 각 질병에 대하여 장기간의 치료효과를 갖는다는 것을 정확하게 이해할 수 있었다고 보기 어렵다. 라) 추가 실험자료에 기초한 피고의 주장 또한, 피고는 “이 사건 정정발명의 ‘실시예 1-68’의 제형을 인간에게 투여한 후 190일 동안 옥트레오티드의 혈중농도를 측정하고, 3개월마다 주사하였을 때 예상되는 혈중농도 곡선을 시뮬레이션 소프트웨어를 사용하여 추정함으로써, ‘실시예 1-68’이 3개월마다 투여되는 제형으로서 인간에 대하여도 성공 가능한 것으로 확인되었는데, ‘실시예 1-68’의 토끼 데이터와 ‘실시예 1-10’의 토끼 데이터를 비교하면 ‘실시예 1-10’ 제형 역시 인간에 대한 3개월 제형으로 유효할 것으로 예상된다.”는 취지로 주장하고 있다. 그러나, 피고 주장과 같이 추정할 수 있다고 하더라도, 피고의 위 주장은 이 사건 정정발명의 우선일 이후 이루어진 실험결과를 기초로 한 것이어서, 이 사건 정정발명의 우선일 당시 통상의 기술자가 과도한 실험이나 특수한 지식을 부가하지 않고서도 인식할 수 있었던 사항이라고 보기는 어렵다. 마) 종래 기술과 비교한 특유한 효과의 기재 이 사건 정정발명의 명세서에는 ‘단일 중합체만을 함유하는 제제(식별번호 [0022]) 등 종래 기술과 비교하였을 때의 차이점(예를 들어 시간․농도 데이터를 비교하여 차이점을 기재할 수 있을 것이다), 그와 같은 차이점을 기초로 서방형 제제로서의 효과가 있다고 판단한 근거’ 등 이 사건 각 정정청구항이 종래 기술과 비교하여 특유한 효과가 있음을 명확하게 인식할 수 있는 기재를 발견하기도 어렵다. 바) 종합 위 가)항 내지 마)항과 같은 사정들을 종합하면, 통상의 기술자로서는 이 사건 각 정정청구항의 실시에 앞서 이 사건 각 정정청구항의 조성물이 이 사건 각 질병에 대하여 서방형 제제로서의 효과를 갖고 있는지에 대한 확인 작업이 필요할 것으로 보인다. 즉 통상의 기술자로서는 비교실험 등의 실험을 통해 직접 서방형 제제로서의 효과를 확인하거나, 통상의 기술자의 수준을 뛰어 넘는 해박한 약리학 등에 대한 지식이 있어야(이와 같은 약리학 등에 대한 지식에 일정한 실험이 추가로 필요할 수도 있을 것이다) ‘이 사건 시간․농도 데이터’의 약물 방출 양상이 서방형 제제로서의 효과가 있는지 여부를 정확하게 이해할 수 있을 것으로 보인다. 그렇다면, 통상의 기술자가 ‘이 사건 시간․농도 데이터’ 등 이 사건 정정발명의 명세서 기재에 의하여 우선일 당시의 기술수준으로 보아 특수한 지식이나 과도한 실험을 거치지 않고 이 사건 각 정정청구항의 옥토레오티드 서방형 제제가 갖는 효과를 정확하게 이해할 수 있다고 보기 어렵다. [이와 같이 보게 되는 경우 제형발명의 명세서 기재요건을 의약의 용도발명과 같은 정도로 보게 된다는 비판이 있을 수 있다. 그러나, 이 사건에 있어서는 이 사건 각 정정청구항의 옥토레오티드 서방형 제제가 위에서 본 바와 같이 수개월의 시간 동안 일자별로 다른 수준의 혈중농도를 갖고 있고 특정 일자에 있어서는 혈중농도가 0인 경우도 있는 반면, 통상의 기술자가이 사건 정정발명의 우선일 당시 토끼에 대한 시간․농도데이터로부터 인간에 대한 장기간의 치료 효과를 판단하거나 토끼에 대한 시간․농도데이터를 기초로 인간에 대한 혈중농도 양상을 추정하기 어려운 등의 사정으로 인해, ‘이 사건 시간․농도 데이터’로부터 서방형 제제로서의 이 사건 각 정정청구항의 효과를 예측 내지 유추하는 것이 어렵다는 이유로 일정한 정도의 명세서 기재요건을 요구하는 것이다. 위와 같은 예측가능성 또는 유추가능성의 제약으로 인해 통상의 기술자로서는 이 사건 각 정정청구항의 실시에 앞서 이 사건 각 질병에 대하여 서방형 제제로서의 효과를 갖고 있는지에 관한 확인을 위하여 많은 시간과 비용 및 노력을 들여야 할 것으로 보이고, 이 사건 각 정정청구항의 발명으로서의 본질은 이 사건 각 질병에 대하여 서방형 제제로서 장기간의 치료 효과를 갖는다는 것에 있는데, 이와 같은 발명을 공개하는 대가로 독점권인 특허권을 부여받으면서 위 발명을 실시하려는 자에게 많은 시간과 비용 및 노력을 들어 효과를 확인하도록 하는 것은 특허법의 취지에 맞지 않는 것으로 보인다. 한편, 이 사건에서 반드시 의약의 용도발명과 같은 수준의 기재가 있어야 명세서 기재요건이 충족되었다고 본 것은 아니다{(위라)항 참조}.] 라. 소결론 따라서, 이 사건 정정발명의 설명에는 통상의 기술자가 이 사건 각 정정청구항을 용이하게 실시할 수 있을 정도로 그 발명의 효과가 기재되어 있지 않으므로, 이 사건 각 정정청구항은 구 특허법 제42조 제3항의 규정에 위배되므로 그 등록이 무효로 되어야 한다. |
| 결론 | 그렇다면, 이와 결론을 달리한 이 사건 심결은 위법하고, 이 사건 심결의 취소를 구하는 원고의 이 사건 청구는 나머지 무효 사유에 관하여 살필 필요 없이 이유 있으므로, 이를 인용하기로 주문과 같이 판결한다. |
[정정청구항]

[기재표]

[표 4]

| 번호 | 사건번호 | 제목 | 분야 | 출원번호 | 법원명 | 날짜 | 조회 수 |
|---|---|---|---|---|---|---|---|
| 154 | 2015허4569 등록무효(특) | 2015허4569 등록무효(특) | 특허/실용신안 | 제756225호 | 특허법원 | 2020.06.19 | 65 |
| 153 | 2015허1133 거절결정(특) |
2015허1133 거절결정(특)
|
특허/실용신안 | 제10-2012-31752호 | 특허법원 | 2020.06.18 | 70 |
| 152 | 2015허3450 거절결정(특) |
2015허3450 거절결정(특)
|
특허/실용신안 | 제10-2006-0103794호 | 특허법원 | 2020.06.18 | 64 |
| 151 | 2015허2587 거절결정(특) |
2015허2587 거절결정(특)
|
특허/실용신안 | . | 특허법원 | 2020.06.18 | 101 |
| 150 | 2015허1836 권리범위확인(특) |
2015허1836 권리범위확인(특)
|
특허/실용신안 | 제981761호 | 특허법원 | 2020.06.18 | 91 |
| 149 | 2015허3283 권리범위확인(특) |
2015허3283 권리범위확인(특)
|
특허/실용신안 | 제10-1385449호 | 특허법원 | 2020.06.18 | 62 |
| » | 2014허3590 등록무효(특) |
2014허3590 등록무효(특)
|
특허/실용신안 | 제1245919호 | 특허법원 | 2020.06.18 | 75 |
| 147 | 2014허4913 등록무효(특) |
2014허4913 등록무효(특)
|
특허/실용신안 | 제0885129호 | 특허법원 | 2020.06.18 | 74 |
| 146 | 2014허4418 거절결정(특) | 2014허4418 거절결정(특) | 특허/실용신안 | 제10-2012-46960호 | 특허법원 | 2020.06.17 | 76 |
| 145 | 2015허277 권리범위확인(특) |
2015허277 권리범위확인(특)
|
특허/실용신안 | 제1263620호 | 특허법원 | 2020.06.17 | 63 |
| 144 | 2015허215 권리범위확인(실) |
2015허215 권리범위확인(실)
|
특허/실용신안 | 제451329호 | 특허법원 | 2020.06.17 | 54 |
| 143 | 2014허8441 권리범위확인(실) |
2014허8441 권리범위확인(실)
|
특허/실용신안 | 제466283호 | 특허법원 | 2020.06.17 | 62 |
| 142 | 2015허659 등록무효(특) |
2015허659 등록무효(특)
|
특허/실용신안 | 제10-1378612호 | 특허법원 | 2020.06.17 | 63 |
| 141 | 2015허154 등록무효(특) |
2015허154 등록무효(특)
|
특허/실용신안 | 제1373142호 | 특허법원 | 2020.06.17 | 71 |
| 140 | 2014허7509 권리범위확인(특) |
2014허7509 권리범위확인(특)
|
특허/실용신안 | 제1178877호 | 특허법원 | 2020.06.17 | 52 |
| 139 | 2014허8878 등록무효(실) |
2014허8878 등록무효(실)
|
특허/실용신안 | 제20-365414호 | 특허법원 | 2020.06.17 | 48 |
| 138 | 2014허7325 등록무효(특) |
2014허7325 등록무효(특)
|
특허/실용신안 | 제971555호 | 특허법원 | 2020.06.17 | 34 |
| 137 | 2014허5794 등록무효(특) |
2014허5794 등록무효(특)
|
특허/실용신안 | 제316401호 | 특허법원 | 2020.06.17 | 53 |
| 136 | 2015허3795 등록정정(특) |
2015허3795 등록정정(특)
|
특허/실용신안 | 제10-0707547호 | 특허법원 | 2020.06.17 | 31 |
| 135 | 2015허1256 거절결정(특) |
2015허1256 거절결정(특)
|
특허/실용신안 | 제10-0540033호 | 특허법원 | 2020.06.17 | 64 |