Extra Form
| 사건번호 |
2014허5817 등록무효(특) |
| 판례제목 |
2014허5817 등록무효(특) |
| 출원번호 |
제10-0656716호 |
| 분야 |
특허/실용신안 |
| 판결일 |
2015-08-13 |
| 법원명 |
특허법원 |
| 원고 |
다이이찌 산쿄 가부시키가이샤 |
| 피고 |
제이더블유중외제약 주식회사, 국제약품공업 주식회사, 대화제약 주식회사, 동아에스티 주식회사, 안국약품 주식회사, 우리들제약 주식회사, 일동제약 주식회사, 일양약품 주식회사, 주식회사 제이알피, 코오롱제약 주식회사, 주식회사 파마킹, 주식회사 하원제약, 주식회사 테라젠이텍스, 주식회사 종근당, 주식회사 경보제약, 주식회사 다산메디켐, 주식회사 바이넥스 |
| 판사 |
한규현, 손천우, 윤주탁 |
| 판결결과 |
등록무효 |
| 주문 |
1, 원고의 피고들에 대한 청구를 모두 기각한다.
2. 소송비용은 원고가 부담한다. |
| 청구취지 |
특허심판원이 2014. 6. 13. 2013당2478, 2013당2479(병합), 2013당2480(병합), 2013당2481(병합), 2013당2482(병합), 2013당2483(병합), 2013당2485(병합), 2013당2486(병합), 2013당2487(병합), 2013당2488(병합), 2013당2489(병합), 2013당2490(병합), 2013당2536(병합), 2013당2618(병합), 2013당2660(병합), 2013당2880(병합), 2013당2890(병합) 사건에 관하여 한 심결을 취소한다. |
| 기초사실 |
1. 기초사실
가. 이 사건 특허발명
1) 발명의 명칭 : 의약 조성물
2) 국제출원일/ 우선권주장일/ 특허법 제203조의 서면 제출일/ 등록일/ 등록번호 : 2001. 11. 19./ 2000. 11. 21./ 2003. 5. 19./ 2006. 12. 6./ 제10-0656716호
3) 특허권자 : 원고
4) 특허청구범위
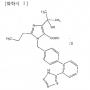
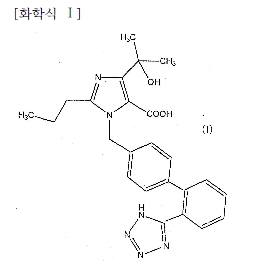
【청구항 1】하기 일반식 (Ⅰ) :
[화학식 Ⅰ]
을 갖는 화합물, 그 약리상 허용되는 염, 그 약리상 허용되는 에스테르 또는 그 약리상 허용되는 에스테르의 약리상 허용되는 염으로 이루어지는 군에서 선택되는 안지오텐신 Ⅱ 수용체 길항제 및 1종 이상의 이뇨제를 유효성분으로 함유하는 고혈압증의 치료 또는 예방용 의약 조성물로서, 상기 1종 이상의 이뇨제가 티아지드계 유도체로부터 선택되는 것인 의약 조성물
【청구항 2】제1항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물 또는 그 약리상 허용되는 에스테르인 의약 조성물.
【청구항 3】제1항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물의 약리상 허용되는 에스테르인 의약 조성물.
【청구항 4】제1항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물의 피발로일옥시메틸에스테르, 프탈리딜에스테르 또는 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸에스테르인 의약 조성물.
【청구항 5】제1항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물의 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸에스테르인 의약 조성물.
【청구항 6】~ 【청구항 11】삭제
【청구항 12】제1항 내지 제5항 중 어느 한 항에 있어서, 이뇨제가 히드로클로로티아지드, 메틸클로티아지드, 벤질히드로클로로티아지드, 트리클로로메티아지드, 시클로 펜티아지드, 폴리티아지드, 에티아지드, 시클로티아지드, 벤드로플루메티아지드 또는 히드로플루메티아지드인 의약 조성물.
【청구항 13】제1항 내지 제5항 중 어느 한 항에 있어서, 이뇨제가 히드로클로로티아지드인 의약 조성물.
【청구항 15】제1항 내지 제5항 중 어느 한 항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물의 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸에스테르이고, 이뇨제가 히드로클로로티아지드이며, 의약 조성물이 온혈 동물의 고혈압증을 예방 또는 치료하기 위 한 것인 의약 조성물.
【청구항 16】제1항 내지 제5항 중 어느 한 항에 있어서, 안지오텐신 Ⅱ 수용체 길항제가 일반식 (I)을 갖는 화합물의 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸에스테르이고, 이뇨제가 히드로클로로티아지드이며, 의약 조성물이 인간의 고혈압증을 예방 또는 치료하기 위한 것인 의약 조성물.
【청구항 17】~ 【청구항 46】삭제
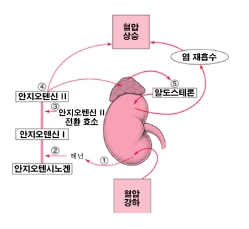
5) 배경기술의 이해
가) 안지오텐신 II의 혈압 상승기전
① 동맥 내의 혈액량이 감소하면 신장에서 레닌이 분비된다.
② 레닌이 혈액속의 안지오텐시노겐(Angiotensinogen : 혈장단백질)을 안지오텐신 I(Angiotensin I)으로 변화시킨다.
③ 안지오텐신 I은 안지오텐신 전환효소(Angiotensin Converting Enzyme, ACE로 약칭됨)에 의해 안지오텐신 II(Angiotensin Ⅱ)로 전환된다.
④ 안지오텐신 Ⅱ는 AT1 수용체와 결합하여 혈관을 수축시킨다.
⑤ 안지오텐신 Ⅱ의 농도가 증가하면 부신에서 알도스테론(Aldosterone)의 분비가 증가하게 되는데, 알도스테론은 신장에서의 염분과 수분의 재흡수를 도와줌으로써 혈액량을 증가시켜 혈압을 상승시킨다.
나) 안지오텐신 Ⅱ 수용체 길항제
안지오텐신 Ⅱ 수용체 길항제는 안지오텐신 Ⅱ가 AT1 수용체에 결합하는 것을 방해함으로써[위 가)항의 ④항 참조] 혈압을 낮추게 된다. 안지오텐신 Ⅱ 수용체 길항제(Angiotensin Ⅱ Receptor Antagonist)는 ‘Angiotensin Aeceptor Blockers’로도 불린다.
6) 발명의 개요 (구체적인 내용은 [별지 1]과 같다)
본 발명은 CS-866 등 특정 안지오텐신 Ⅱ 수용체 길항제와 이뇨제를 유효성분으로 함유하는 고혈압증의 예방 또는 치료를 위한 의약 조성물에 관한 것이다.
본 발명의 의약 조성물의 유효성분은 청구항 1 기재 일반식 (Ⅰ)을 갖는 화합물, 그 약리상 허용되는 염, 그 약리상 허용되는 에스테르 또는 그 약리상 허용되는 에스테르의 약리상 허용되는 염으로 이루어지는 군에서 선택되는 안지오텐신 Ⅱ 수용체 길항제와 1 종 또는 2 종 이상의 이뇨제로 이루어진다.
나. 선행발명들
1) 선행발명 1 (갑 제4호증)
가) 명칭 : 안지오텐신 Ⅱ 수용체 길항제 (Angiotensin Ⅱ Receptor Antagonists)
나) 공개일/ 공개 간행물 : 2000. 5. 22./ Mancia Giuseppe, et al., Informa Healthcare (2nd edition)
다) 발명의 개요
선행발명 1은 안지오텐신 Ⅱ 수용체 길항제에 관한 것이다. 안지오텐신 Ⅱ 수용체 길항제의 비교 약리학, 고혈압 치료에서의 단독요법으로서의 안지오텐신 Ⅱ 수용체 길항제의 용도, 고혈압에 대한 조합 치료에서의 안지오텐신 Ⅱ수용체 길항제의 용도 등이 기재되어 있는 단행본이다.
고혈압 치료의 위 조합 치료에 관한 부분에는 안지오텐신 Ⅱ 수용체 길항제와 이뇨제의 조합 치료가 유용한 것으로 기재되어 있는데, 그 구체적인 사례로 안지오텐신 Ⅱ 수용체 길항제인 로사르탄, 칸데사르탄, 이르베사르탄, 발사르탄과 이뇨제인 히드로클로로티아지드(이하 ‘HCTZ’라 한다)의 조합 치료에 관한 임상효과가 기재되어 있다(이하 안지오텐신 Ⅱ 수용체 길항제와 HCTZ의 병용제를 ‘ARB 병용제’라 한다).
한편, 미등록 실험 화합물들이 열거된 표 2.1에는 CS-866이 기재되어 있다.
2) 선행발명 2 (을나 제1호증)
가) 명칭 : 고혈압에 있어서 안지오텐신 Ⅱ 수용체 길항제의 임상적 약물동력학[Clinical pharmacokinetics of angiotensin II(AT1) receptor blockers in hypertension]
나) 공개일/ 공개 간행물 : 2000. 4./ Journal of Human Hypertension 2000, Suppl. 1, S73-S86
다. 심결의 경위
1) 원고를 상대로 특허심판원에, 피고 제이더블유중외제약 주식회사는 2013당2478호로, 피고 국제약품 주식회사는 2013당2479호로, 피고 대화제약 주식회사는 2013당2480호로, 피고 동아에스티 주식회사 2013당2481호로, 피고 안국약품 주식회사는 2013당2482호로, 피고 우리들제약 주식회사는 2013당2483호로, 피고 일동제약 주식회사는 2013당2485호로, 피고 일양약품 주식회사는 2013당2486호로, 피고 주식회사 제이알피는 2013당2487호로, 피고 코오롱제약 주식회사는 2013당2488호로, 피고 주식회사 파마킹은 2013당2489호로, 피고
주식회사 하원제약은 2013당2490호로, 피고 주식회사 테라젠이텍스는 2013당2536호로, 피고 주식회사 종근당은 2013당2618호로, 피고 주식회사 경보제약은 2013당2660호로, 피고 주식회사 다산메디켐은 2013당2890호로, 피고 주식회사 바이넥스는 2013당2880호로 각 이 사건 특허발명에 대한 무효심판을 청구하였다(이하 피고들의 명칭 중 ‘주식회사’는 생략한다).
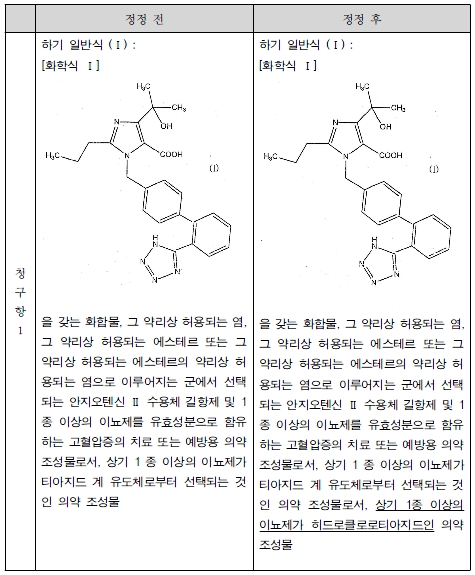
2) 원고는 위 각 무효심판절차에서 아래 표 기재와 같이 청구항 1을 정정하고 청구항 12, 13을 삭제하는 내용의 정정청구를 하였다(밑줄 친 부분이 정정을 구하는 부분이다. 이하 ‘이 사건 정정청구’라 하고, 정정청구 후의 특허발명의 각 청구항을 ‘정정청구항 1’과 같은 방법으로 표시하며, 정정청구된 전체 발명을 칭할 때는 ‘이 사건 정정청구발명’이라 한다).
3) 특허심판원은 위 각 무효심판청구사건을 병합하여 심리한 다음 2014. 6. 13. “이 사건 정정청구를 인정한다. 정정청구항 1은 선행발명 1에 의하여 신규성이 부정되지는 않는다. 그러나 정정청구항 1은 선행발명 1에 대한 선택발명으로서 선행발명 1과 질적으로 다른 효과를 갖고 있거나 양적으로 현저한 차이가 있다고 보기는 어려우므로, 선행발명 1의 선택발명으로서의 진보성이 부정된다. 정정청구항 1의 종속항인 정정청구항 2 내지 5는 정정청구항 1에서 본 바와 같은 이유로 선행발명 1에 의하여 진보성이 부정된다. 정정청구항 1 내지 5의 종속항인 정정청구항 15, 16은 정정청구항 1 내지 5에서 본 바와 같은 이유로 선행발명 1에 의하여 진보성이 부정된다. 따라서, 정정청구항 1 내지 5, 15, 16은 그 등록이 무효로 되어야 한다.”는 이유로 피고들의 심판청구를 인용하는 이 사건 심결을 하였다.
[인정근거] 갑 제1 내지 4호증, 을나 제1호증의 각 기재, 변론 전체의 취지 |
| 원고의 주장요지 |
1) 이 사건 심결의 판단에 대하여
가) 이 사건 정정청구발명은 선행발명 1과의 관계에서 선택발명에 해당하지 않는다.
나) 선행발명 1에 의하여 안지오텐신 II 수용체 길항제와 HCTZ의 병용제가 알려져 있었다고 하더라도, CS-866은 종래의 안지오텐신 II 수용체 길항제와 비교하여 필수 작용기의 구조가 다른바, 이 사건 정정청구발명의 기술분야에서 통상의 지식을 가진 사람(이하 ‘통상의 기술자’라 한다)이 선행발명 1에 나타나 있는 수십 종의 화합물 중 CS-866을 선택하여 HCTZ와 병용함으로써 상승적 혈압 강하 효과가 얻어질 것이라고 예상할 수 없다. 따라서, 통상의 기술자가 선행발명 1로부터 이 사건 정정청구발명의 CS-866과 HCTZ의 병용제(이하‘이 사건 병용제’라 한다) 구성을 용이하게 도출할 수 없다.
다) 이 사건 병용제는 종래의 ARB 병용제에 비하여 상승효과 등의 현저한 효과가 있다.
(1) 통상의 기술자는 이 사건 정정청구발명의 명세서 기재에 의하여 이 사건 병용제의 상승효과22)를 인식할 수 있다(이 사건 정정청구발명의 실시예에서의 효과가 유의한 상승효과로 보기 어려운 것은 ➀ 단독으로도 상당한 혈압강하를 나타내는 고용량의 HCTZ가 사용되었을 뿐만 아니라 ➁ 병용에 의하여 혈압이 정상수치까지 내려감으로써 더 이상의 혈압 강하 효과가 나타나기 힘든 실험조건에 기인한 것이므로, 이와 같은 실험조건을 감안하면 통상의 기술자는 이 사건 정정청구발명 명세서의 데이터를 상승효과라고 인식할 수 있다).
(2) 이 사건 정정청구발명의 명세서에 기재되어 있는 데이터를 CI23)에 의하여 평가하는 경우 상승효과를 나타내는 것으로 평가된다.
(3) 종래의 ARB 병용제는 상승효과가 없는 반면, 원고가 제출한 비교실험자료와 우선일 이후의 문헌에 의하면, 이 사건 병용제는 종래의 ARB 병용제에 비하여 혈압 강하와 조절에 있어 현저한 효과가 있다.
라) 이 사건 병용제는 당뇨병성 신증의 발병시간을 늦추는 효과가 있어, 종래의 ARB 병용제로부터 예측할 수 없는 이질적인 효과도 갖는다.
마) 따라서, 정정청구항 1 내지 5, 15, 16은 선행발명 1과 대비하여 선택발명에 해당하지 않고, 구성의 곤란성이 있을 뿐만 아니라 현저한 효과 내지 이질적인 효과가 있으므로, 선행발명 1에 의하여 진보성이 부정되지 않는다.
2) 피고 주식회사 바이넥스의 주장에 대하여
선행발명 2에는 잠재적인 안지오텐신 II 수용체 길항제로서 연구 중인 28개의 화합물 중 하나로서 CS-866이 개시되어 있을 뿐이어서, 이 사건 정정청구발명의 병용제의 구성을 직접적으로 인식할 수 없으므로, 정정청구항 1 내지 5, 15, 16은 선행발명 2에 의하여 신규성이 부정되지 않는다.
3) 심결의 위법
따라서, 이와 결론을 달리하여 선행발명 1에 의하여 정정청구항 1 내지 5, 15, 16의 진보성이 부정된다고 판단한 이 사건 심결은 위법하므로 취소되어야 한다. |
| 당사자의 주장 요지 |
<피고 제이더블유중외제약, 대화제약, 동아에스티, 우리들제약, 일동제약, 일양약품, 파마킹, 하원제약, 테라젠이텍스, 다산메디켐 주장의 요지>
1) 이 사건 병용제를 조성물로 하는 정정청구항 1 내지 5, 15, 16은 선행발명 1과의 관계에서 선택발명에 해당한다. 이 사건 병용제는 선행발명 1에 비하여 현저한 효과를 갖지 않는다. 따라서, 정정청구항 1 내지 5, 15, 16은 선행발명 1에 의하여 진보성이 부정된다.
2) 설령 이 사건 병용제를 조성물로 하는 정정청구항 1 내지 5, 15, 16이 선행발명 1과의 관계에서 선택발명에 해당하지 않는다고 하더라도, 통상의 기술자가 선행발명 1로부터 이 사건 병용제의 구성을 용이하게 도출할 수 있다. 또한 이 사건 병용제는 선행발명 1에 비하여 현저한 효과를 갖지 않는다. 따라서, 정정청구항 1 내지 5, 15, 16은 선행발명 1에 의하여 진보성이 부정된다.
3) 따라서, 이 사건 심결은 이와 결론을 같이하여 적법하다.
<피고 코오롱제약 주장의 요지>
이 사건 병용제는 종래의 ARB 병용제에 비하여 현저한 효과가 없어, 이 사건 병용제를 조성물로 하는 정정청구항 1 내지 5, 15, 16은 선행발명 1에 의하여 진보성이 부정된다.
따라서, 이 사건 심결은 이와 결론을 같이하여 적법하다.
<피고 바이넥스 주장의 요지>
이 사건 병용제를 조성물로 하는 정정청구항 1 내지 5, 15, 16은 선행발명 2에 의하여 신규성이 부정된다.
따라서, 이 사건 심결은 이와 결론을 같이하여 적법하다. |
| 이 사건 심결의 당부에 대한 판단 |
<이 사건 심결의 위법 여부>
가. 이 사건 정정청구발명의 분석
정정청구항 1은 ‘[화학식 I]을 갖는 화합물, 그 약리상 허용되는 염, 그 약리상 허용되는 에스테르 또는 그 약리상 허용되는 에스테르의 약리상 허용되는 염으로 이루어지는 군에서 선택되는 안지오텐신 II 수용체 길항제 및 1종 이상의 이뇨제를 유효성분으로 함유하는 고혈압증의 치료 또는 예방용 의약 조성물로서, 상기 1종 이상의 이뇨제가 HCTZ인 의약 조성물’이다. 한편, 이 사건 정정청구발명 명세서에는 정정청구항 1의 ‘[화학식 I]을 갖는 화합물, 그 약리상 허용되는 염, 그 약리상 허용되는 에스테르 또는 그 약리상 허용되는 에스테르의 약리상 허용되는 염으로 이루어지는 군에서 선택되는 안지오텐신 II 수용체 길항제’와 관련하여, “본 발명의 유효성분인 안지오텐신 II 수용체 길항제는 바람직하게는 화합물 (I) 또는 그 약리상 허용되는 에스테르이며, 더욱 바람직하게는 화합물 (I)의 약리상 허용되는 에스테르이며, 더욱 더 바람직하게는 화합물 (I)의 피발로일옥시메틸에스테르, 프탈리딜에스테르 또는 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸에스테르이며, 가장 바람직하게는 (5-메틸-2-옥소-1,3-디옥솔렌-4-일)메틸4-(1-히드록시-1-메틸에틸)-2-프로필-1-[2'-(1H-테트라졸-5-일)비페닐-4-일메틸]이미다졸-5-카르복실레이트(CS-866)이다.”(갑제3호증 8면 3단락)라고 기재되어 있다.
따라서, 정정청구항 1은 이 사건 병용제(CSS-866과 HCTZ의 병용제)를 조성물로 하고, 인간의 고혈압의 예방 또는 치료를 의약용도로 하는 의약용도발명(이하 ‘이 사건 병용제 포함 발명’이라 한다)을 보호범위에 포함하고 있다. 또한, 정정청구항 1을 한정하고 있는 정정청구항 1의 종속항인 정정청구항 2 내지 5, 15, 16도 '이 사건 병용제 포함 발명'을 보호범위에 포함하고 있다(당사자들 사이에 특별한 다툼이 없다).
아래에서는 정정청구항 1 내지 5, 15, 16 중 '이 사건 병용제 포함 발명'의 진보성이 부정되는지에 관하여 보기로 한다.
나.‘이 사건 병용제 포함 발명’과 선행발명 1의 대비 : 공통점과 차이점
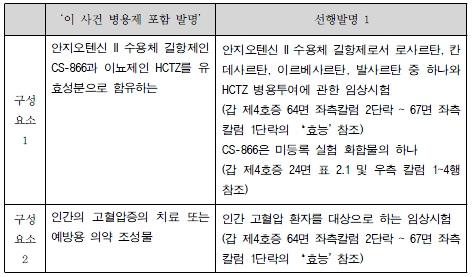
정정청구항 1 중 ‘이 사건 병용제 포함 발명’과 선행발명 1을 구성요소별로 대비하여 보면 아래 대비표와 같다.
위 대비표에 근거하여 ‘이 사건 병용제 포함 발명’과 선행발명 1의 대응구성과 의 공통점, 차이점을 살펴보기로 한다. 양 발명은 안지오텐신 II 수용체 길항제(‘이 사건 병용제 포함 발명’에서는 CS-866, 선행발명 1에서는 로사르탄 등)와 이뇨제인 HCTZ를 조성물(‘ARB 병용제’)로 하고 의약용도를 인간 고혈압의 예방 또는 치료로 한다는 점에서 공통점이 있다. 다만 ‘이 사건 병용제 포함 발명’에서는 안지오텐신 Ⅱ 수용체 길항제로서 CS-866을 포함하고 있는 반면, 선행발명 1에서는 안지오텐신 Ⅱ 수용체 길항제로서 로사르탄 등을 포함하고 있다는 점에서 차이가 있다.
따라서, 아래에서는 통상의 기술자가 그러한 차이에도 불구하고 선행발명 1로부터 ‘이 사건 병용제 포함 발명’의 구성(이 사건 병용제)을 용이하게 도출할 수 있는지, ‘이 사건 병용제 포함 발명’이 선행발명 1에 비하여 효과의 현저성이 있는지를 살펴봄으로써, 통상의 기술자가 선행발명 1로부터 ‘이 사건 병용제 포함 발명’을 용이하게 발명할 수 있는지를 판단하기로 한다.
다.‘이 사건 병용제 포함 발명’과 선행발명 1의 차이점에 대한 검토
1) 구성의 용이 도출 여부
아래와 같은 사정들을 종합하면, 통상의 기술자가 선행발명 1과의 차이에도 불구하고, 선행발명 1로부터, 안지오텐신 Ⅱ 수용체 길항제인 CS-866과 이뇨제인 HCTZ를 조성물로 하고, 의약용도를 인간의 고혈압을 예방 또는 치료로 하는 ‘이 사건 병용제 포함 발명’의 구성을 용이하게 도출할 수 있다.
① 선행발명 1에는 “고혈압 치료를 위하여 안지오텐신 Ⅱ 수용체 길항제가 매우 효과적으로 이뇨제와 조합되는데, 이는 이뇨제에 의해 유발된 RAS 자극에 대항하는 안지오텐신 길항제의 능력을 기초로 한다.”는 취지로 기재되어 있다. 또한, 선행발명 1에서는 “이뇨제는 체내 나트륨을 감소시킴으로써 혈압을 강하시키는데, 이와 같이 체내 나트륨이 감소되면 레닌 방출이 과하게 증가하여 고혈압이 지속되는바, 이뇨제 치료와 동시에 레닌-안지오텐신 시스템을 차단하면 과(過)레닌혈증을 억제하여 나트륨 감소에 의한 최선의 혈압 강하 효과를 얻을 수 있다.”는 취지로 위와 같은 효과에 대한 약리학적 근거를 제시하고 있다(아래 상자의 선행발명 1 기재 참조).
② 더욱이 선행발명 1에는 안지오텐신 Ⅱ 수용체 길항제인 로사르탄, 발사르탄, 이르베사르탄과 HCTZ의 병용제인 의약품이 미국에서 시판되고 있고, 이와 같은 클래스의 다른 약물이 뒤따를 것이며, 안지오텐신 Ⅱ 수용체 길항제와 HCTZ를 포함하는 고정 복용량 조합은 1차적 치료법으로도 사용이 증가될 것이라고 기재되어 있다(아래 상자의 선행발명 1 기재 참조).
③ 선행발명 1에서는 안지오텐신 Ⅱ 수용체 길항제의 예를 표 2.1에 열거하면서, 등록된 화합물인 로사르탄, 발사르탄, 칸데사르탄, 텔미사르탄, 에프로사르탄과 함께 미등록 실험 화합물의 하나로 CSS-866을 들고 있다. 또한 선행발명 1에는 “안지오텐신 Ⅱ 수용체 길항제가 항고혈압 약물로 개발되고 등록되었다.”고 기재되어 있다(아래 상자의 선행발명 1 기재 참조).
④ 비록 미등록 실험 화합물이기는 하나 선행발명 1에 CS-866이 안지오텐신 Ⅱ 수용체 길항제의 하나로 기재되어 있고, 안지오텐신 Ⅱ 수용체 길항제는 안지오텐신 Ⅱ가 AT1 수용체에 결합하는 것을 방해함으로써 항고혈압 작용을 하는 약리기전을 갖는 것으로 통상의 기술자에게 인식되어 있는 이상, CS-866이 로사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제와 비교하여 화학 구조가 다르다고 하더라도, 안지오텐신 Ⅱ 수용체 길항제인 CS-866과 이뇨제인 HCTZ로 이루어진 조성물의 구성을 도출하거나 위 조성물의 인간의 고혈압증에 관한 약리효과를 예측함에 있어 방해가 된다고 보기 어렵다.
2) 효과의 현저성 여부
아래와 같은 사정들을 종합하면, '이 사건 병용제 포함 발명'이 선행발명 1에 비하여 예측할 수 없는 현저한 상승효과를 갖는다거나 이질적인 효과를 갖는다고 보기 어렵다.
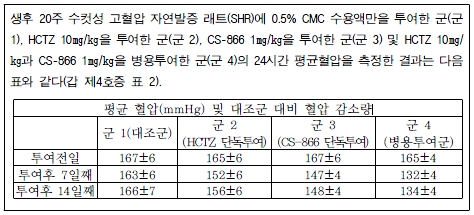
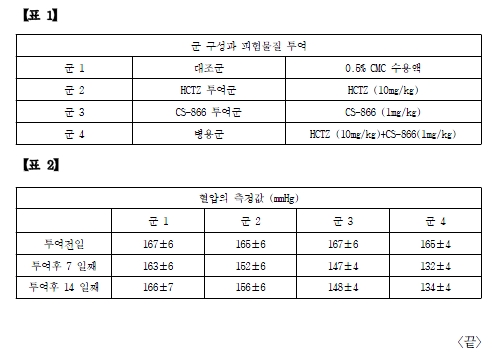
① 이 사건 정정청구발명의 명세서에 기재된 실험결과(아래 상자 참조)는 ‘이 사건 병용제 포함 발명’이 ‘로사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’와 비교하여 현저한 상승효과를 갖는 기재로 보기 어렵다[원고 주장과 같이 ‘병용투여의 경우 대조군과의 차이’가 ‘각 단독투여에 있어서의 대조군과의 차이들의 합계’보다 크다고 하더라도(7일째의 경우 병용투여의 경우 -29, 단독투여의 합 -25, 14일째의 경우 병용투여의 경우 -30, 단독투여의 합 -26) 위 표에 나타난 평균 혈압의 표준오차(±4 내지 ±7까지)를 감안하면, 병용투여군의 효과가 상승효과를 나타낸 것이라고 보기 어렵다. 더욱이 원고가 전문가 의견으로 제출한 진술서에서도 이 사건 정정청구발명의 위 실험결과에 대하여 “상승효과를 보여주고 있지만, 통계적으로 유의하지 않다.”는 취지로 기재되어 있다(갑 제14호증 23면 7.1항 참조)].
② 갑 제8 내지 14, 17호증의 각 기재만으로는 ‘이 사건 병용제 포함 발명’이 선행발명 1에 비하여 현저한 상승효과가 있다고 보기 어렵다. 즉 원고가 제출한 위 각 증거는 이 사건 병용제가 상승효과가 있는지를 단독투여의 경우와 비교하거나 ‘CSS-866과 다른 이뇨제의 병용투여’와 비교한 실험결과에 불과할 뿐 ‘로사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’와 비교하여 상승효과를 평가한 실험결과가 아니거나(갑 제8 내지 10, 12, 13호증), ‘이 사건 병용제 포함 발명’만의 CI 지수를 평가한 것에 불과할 뿐 ‘로사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’와 비교하여 CI 지수를 비교 평가한 것이 아니거나(갑 제14, 17호증), 동등한 실험조건에서 이루어진 것 이라고 보기 어려운 비교 실험결과이다(갑 제11호증).
③ 갑 제19 내지 21호증에는 ‘이 사건 병용제 포함 발명’이 ‘종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’에 포함되는 ‘발사르탄과 HCTZ 병용제’, ‘이르베사르탄과 HCTZ 병용제’ 등에 비하여 혈압 강하 수치 등에 있어 우수한 효과가 있다는 실험결과가 기재되어 있다. 그러나, 한편 을가 제10, 11호 증에는 ‘식품의약품안전처에서 허가되어 판매 중인 용량(160mg)의 발사르탄’과 HCTZ 병용제, ‘식품의약품안전처에서 허가되어 판매 중인 용량(80mg)의 텔미사르탄’과 HCTZ 병용제가 ‘식품의약품안전처에서 허가되어 판매 중인 용량(20mg)의 CSS-866’과 HCTZ 병용제에 비하여 혈압 강하 수치 등에 있어 우수한 효과가 있다는 실험결과가 기재되어 있다. 이에 비추어 보면, ‘이 사건 병용제 포함 발명’은 CS-866의 용량, 발사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들의 용량에 따라 ‘발사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’에 비하여 혈압 강하 수치 등에 있어 열등한 효과를 보일 수 있다고 할 것이다. 그런데, 정정청구항 1 내지 5, 15, 16에서는 ‘발사르탄 등 종래의 안지오텐신 Ⅱ 수용체 길항제들과 HCTZ 병용제’ 보다 현저한 상승효과를 갖는 투여량을 특별히 한정하고 있지 않다[1개의 특허청구범위의 일부에 공지기술에 의하여 진보성이 부정되는 등의 특허무효의 사유가 있는 경우 그 부분이 나머지 부분과 유기적으로 결합된 것이라고 인정되지 않는 한 그 항의 발명은 전부에 대하여 그 등록이 무효로 되어야 할 것인바(대법원 1998. 9. 18. 선고 96후2395 판결 등 참조), 정정청구항 1 내지 5, 15, 16이 양적으로 현저한 효과가 있다고 인정되지 아니하는 부분을 포함하고 있는 경우에는 정정청구항 1 내지 5, 15, 16의 각 항 전부가 선행발명 1에 의하여 진보성이 부정된다].
④ 원고는 이 사건 병용제가 당뇨병성 신증의 발병을 늦추는 이질적인 효과가 있다는 취지로 주장하나, 원고 주장의 효과는 이 사건 병용제의 의약용도와 관련이 있다고 보기 어려울 뿐만 아니라 이 사건 정정청구발명의 명세서에 원고 주장의 효과와 관련하여 의약용도발명에서의 효과로 인정할만한 기재를 발견하기 어렵다.
라. 대비 결과의 종합
위 대비 결과를 종합하면, ‘이 사건 병용제 포함 발명’은 선행발명 1과 대비하여 구성의 곤란성과 효과의 현저성을 인정하기 어려우므로, 결국 통상의 기술자가 선행발명 1로부터 용이하게 발명할 수 있는 것으로서 그 진보성이 부정된다.
나아가, 1개의 특허청구범위의 일부에 공지기술에 의하여 진보성이 부정되는 등의 특허무효의 사유가 있는 경우 그 부분이 나머지 부분과 유기적으로 결합된 것이라고 인정되지 않는 한 그 항의 발명은 전부에 대하여 그 등록이 무효로 되어야 할 것인바(대법원 1998. 9. 18. 선고 96후2395 판결 등 참조), 정정청구항 1 내지 5, 15, 16에서 위와 같이 진보성이 부정되는 ‘이 사건 병용제 포함 발명’은 나머지 부분과 서로 택일적인 관계에 있을 뿐 유기적으로 결합된 것이 아니므로, 정정청구항 1 내지 5, 15, 16은 전부에 대하여 그 등록이 무효로 되어야 할 것이다.
마. 이 사건 심결의 위법 여부
따라서, 위와 결론을 같이한 이 사건 심결은 적법하다. |
| 결론 |
따라서, 이 사건 심결의 취소를 구하는 원고의 피고들에 대한 각 청구는 이유없어 이를 모두 기각하기로 하여 주문과 같이 판결한다. |




 2015허3795 등록정정(특)
2015허3795 등록정정(특)
 2015허1256 거절결정(특)
2015허1256 거절결정(특)